
 Surveillance du processus de mélange par spectroscopie NIR en ligne
Surveillance du processus de mélange par spectroscopie NIR en ligne
 Visum Palm GxP : Le Nouvel Analyseur NIR pour Industrie Pharmaceutique
Visum Palm GxP : Le Nouvel Analyseur NIR pour Industrie Pharmaceutique

Analyseur de procédé Raman pour la surveillance en temps réel de la rapamycine : des résultats comparables à la HPLC

Analyseur de procédé Raman en ligne appliqué à la purification de la rapamycine
La spectroscopie Raman, lorsqu’elle est mise en œuvre sous la forme d’un analyseur de procédé Raman pour des mesures en temps réel, constitue une technologie puissante pour le contrôle et l’optimisation des procédés dans la fabrication pharmaceutique et biotechnologique. Dans ce contexte, l’analyseur de procédé Raman en ligne développé et fabriqué par IRIS Technology Solutions (Barcelone) se distingue comme une solution analytique haute performance pour la quantification en temps réel de composés critiques et la surveillance continue des performances du procédé.
Contrairement aux techniques analytiques conventionnelles telles que la HPLC, qui impliquent des temps de réponse différés, des consommables et une utilisation intensive des ressources de laboratoire, un analyseur de procédé Raman offre une vision directe et en temps réel du procédé. Cet article présente une application industrielle concrète : l’utilisation de l’analyseur Visum Raman In-Line pour surveiller la concentration de rapamycine durant l’étape de purification.
Les résultats démontrent que cet analyseur de procédé Raman, intégré dans une configuration at-line et monté sur un rack mobile, peut remplacer efficacement l’analyse HPLC hors ligne. L’application a été développée en collaboration avec l’entreprise pharmaceutique MyBiotech GmbH (Allemagne) et illustre la valeur de l’analyse de procédés basée sur le Raman dans le cadre des stratégies PAT.
Procédé d’extraction et de purification de la rapamycine
La rapamycine est un composé macrolide largement utilisé pour prévenir le rejet lors des transplantations d’organes. Elle est produite par fermentation en cultivant Streptomyces rapamycinicus dans des bioréacteurs sous des conditions contrôlées d’alimentation en substrat, de température et de pH. Après la fermentation, la rapamycine est extraite à l’aide d’un solvant organique, ce qui donne un mélange complexe contenant le composé cible et plusieurs sous-produits.
L’extrait est ensuite purifié à l’aide d’une colonne chromatographique, où la rapamycine est séparée des impuretés et collectée en fractions enrichies. Traditionnellement, des aliquotes sont prélevées manuellement à la sortie de la colonne et analysées par HPLC afin de déterminer quelles fractions contiennent de la rapamycine et à quelle concentration.
Pour remplacer ce flux de travail hors ligne, une chambre de mesure dédiée a été installée à la sortie de la colonne chromatographique. Une sonde d’immersion connectée à l’analyseur de procédé Raman a été insérée dans cette chambre, permettant une mesure continue et en temps réel de la concentration de rapamycine. Cette configuration a permis de prendre des décisions immédiates concernant la collecte des fractions, leur classification, la recirculation du solvant ou leur rejet, tout en évitant les erreurs, les retards et les risques de contamination associés à l’échantillonnage manuel.
Intégration de l’analyseur de procédé Raman en ligne
Le Visum Raman In-Line a été déployé comme analyseur de procédé Raman en ligne, configuré en environnement at-line sur un rack mobile. Cette intégration flexible a permis à l’analyseur de fonctionner directement à côté du système de purification, tout en conservant une accessibilité et une visibilité complètes pour les opérateurs.
La sonde Raman a mesuré en continu le flux du procédé à la sortie de la colonne, fournissant un retour en temps réel sur la présence et la concentration de la rapamycine. Lors d’un cycle de séparation typique, pouvant durer plusieurs heures, de nombreuses mesures Raman ont été collectées pour chaque fraction, offrant une résolution temporelle nettement supérieure à celle de l’analyse basée sur la HPLC.
Figure 1.
En haut : système de purification de la rapamycine.
En bas à gauche : sonde Raman insérée dans la chambre de mesure.
En bas à droite : écran de l’analyseur de procédé Raman monté sur un rack mobile, affichant la concentration de rapamycine en temps réel.


Étalonnage et modélisation chimiométrique de l’analyseur de procédé Raman
Pour étalonner l’analyseur de procédé Raman, six préparations différentes ont été évaluées. Ces préparations couvraient une plage de concentrations de rapamycine, de profils de sous-produits et de débits, garantissant une variabilité de procédé réaliste.
L’analyseur a été configuré pour acquérir trois spectres Raman par minute et fournir des valeurs moyennées. Pour le développement du modèle chimiométrique, tous les spectres Raman enregistrés pendant le remplissage de chaque flacon ont été moyennés afin d’obtenir un spectre représentatif correspondant à chaque valeur de référence HPLC.
Des techniques chimiométriques avancées ont été appliquées pour traiter les données spectrales et construire des modèles quantitatifs. Afin de garantir une évaluation réaliste des performances, chaque préparation a été traitée comme un jeu de validation externe. En pratique, le modèle utilisé pour prédire une préparation a été développé à partir des données des cinq autres préparations. Cette approche a été répétée jusqu’à ce que les six préparations soient prédites indépendamment par l’analyseur.
Résultats de l’analyseur de procédé Raman
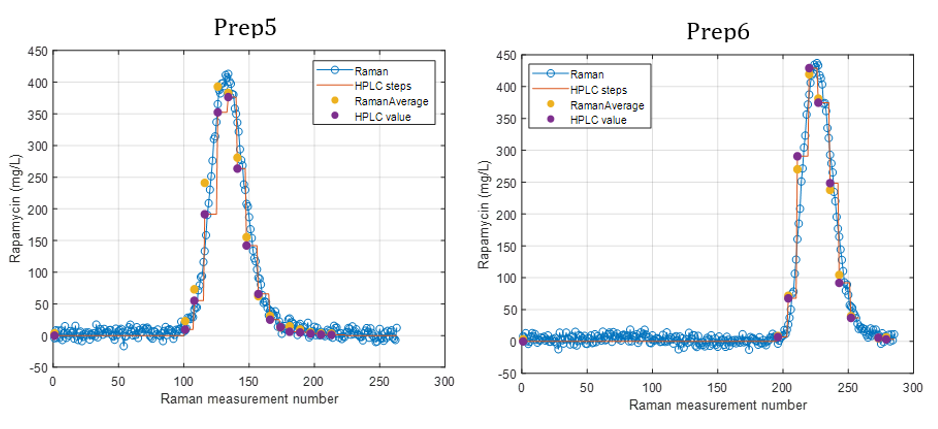
La Figure 2 présente les résultats de prédiction obtenus avec l’analyseur de procédé Raman en ligne pour les six préparations. La tendance de la concentration de rapamycine prédite par la spectroscopie Raman suit étroitement celle mesurée par HPLC.
Pour chaque point de données HPLC, entre trois et huit prédictions Raman étaient disponibles. La moyenne de ces prédictions Raman a montré une forte concordance avec les valeurs HPLC correspondantes. Une divergence a été observée pour la Préparation 3, où un décalage entre la mesure Raman et l’échantillon HPLC collecté s’est probablement produit en raison de différences de synchronisation entre la mesure et la collecte des fractions.
Lorsque l’ensemble des valeurs prédites et de référence a été comparé, l’analyseur a atteint une faible erreur de prédiction de 15,7 mg/L et un coefficient de détermination élevé (R² = 0,98). Cette erreur de prédiction est comparable à la limite de quantification de la méthode.
À des concentrations de rapamycine inférieures à 15 mg/L, les prédictions Raman ont fluctué entre −15 et +15 mg/L, indiquant la limite pratique de détection du modèle. Dans la plage de concentration validée de 15 à 450 mg/L, l’analyseur de procédé Raman en ligne a démontré une excellente précision, avec des résultats très proches de ceux obtenus par HPLC.
Figure 2.
Concentration de rapamycine prédite par l’analyseur de procédé Raman et données de référence HPLC au cours du temps pour les six préparations.

Implications pour l’analyse de procédés Raman et les applications PAT
Cette étude confirme qu’un analyseur de procédé Raman constitue une solution fiable et précise pour la surveillance en temps réel de la purification de la rapamycine. Le Visum Raman In-Line a permis la quantification continue de la rapamycine avec des performances comparables à la HPLC, tout en améliorant significativement l’efficacité et la réactivité du procédé.
En éliminant la nécessité d’un échantillonnage manuel et d’analyses hors ligne, l’analyseur de procédé Raman en ligne Visum a réduit la charge de travail du laboratoire, accéléré la prise de décision et amélioré le contrôle du procédé. Ces avantages rendent l’analyse de procédés basée sur le Raman particulièrement attractive pour la fabrication pharmaceutique et biotechnologique.
Cette approche est entièrement transférable à d’autres applications où la quantification en temps réel pendant la purification ou la formulation est critique, telles que les anticorps, les protéines recombinantes, les vaccins, les métabolites et d’autres principes actifs pharmaceutiques. Dans le cadre d’une stratégie PAT plus large, un analyseur de procédé Raman fournit une vision continue du procédé, permettant une efficacité accrue, un meilleur contrôle de la qualité et des opérations de fabrication plus robustes.



